Equação geral dos gases
Através das três Transformações gasosas (isotérmica, isobárica, isovolumétrica) representadas respectivamente pelas equações: PV = K, V/T = K, P/T = K é que se chegou à Equação geral dos gases:
.jpg) Observe que a equação aborda as três variáveis de estado (P, V e T). Sendo assim, é possível conhecer o volume, a temperatura e pressão de um gás se nos basearmos nessa equação.
Observe que a equação aborda as três variáveis de estado (P, V e T). Sendo assim, é possível conhecer o volume, a temperatura e pressão de um gás se nos basearmos nessa equação.
Vejamos um exemplo:
.jpg)
O diagrama acima representa as transformações de uma massa fixa de gás, baseando-se nele podemos responder às seguintes questões:
- Qual o valor da pressão do gás no ponto A? Repare que o ponto A se localiza no valor 2,0 no vetor P (atm), portanto dizemos que o valor da pressão atmosférica em A é de 2 atm.
- E o valor da pressão no ponto B? Repare que esse ponto se encontra na mesma posição de A em relação ao vetor P (atm). Portanto, B obedece às mesmas condições de A e possui a mesma pressão: 2 atm.
- Qual transformação gasosa ocorre na passagem de A para B?
Transformação Isobárica, pois a pressão do gás é constante (2 atm) e o volume varia, de 4 litros (ponto A) para 8 litros (ponto B).
- E o volume no ponto C? Se subtrairmos B – A, obtemos o volume de C = 4 litros.
- Considerando C e A: a pressão nesses pontos varia, mas o volume não. Temos então uma transformação gasosa Isovolumétrica.
.jpg)
Vejamos um exemplo:
.jpg)
O diagrama acima representa as transformações de uma massa fixa de gás, baseando-se nele podemos responder às seguintes questões:
- Qual o valor da pressão do gás no ponto A? Repare que o ponto A se localiza no valor 2,0 no vetor P (atm), portanto dizemos que o valor da pressão atmosférica em A é de 2 atm.
- E o valor da pressão no ponto B? Repare que esse ponto se encontra na mesma posição de A em relação ao vetor P (atm). Portanto, B obedece às mesmas condições de A e possui a mesma pressão: 2 atm.
- Qual transformação gasosa ocorre na passagem de A para B?
Transformação Isobárica, pois a pressão do gás é constante (2 atm) e o volume varia, de 4 litros (ponto A) para 8 litros (ponto B).
- E o volume no ponto C? Se subtrairmos B – A, obtemos o volume de C = 4 litros.
- Considerando C e A: a pressão nesses pontos varia, mas o volume não. Temos então uma transformação gasosa Isovolumétrica.
Um gás pode passar por três tipos de variáveis de estado: quanto ao seu volume, quanto à temperatura e quanto à pressão. Essas alterações são conhecidas como transformação isobárica, isovolumétrica e isotérmica. A partir dessas três transformações gasosas é que se chegou à equação:
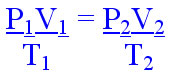
Essa é conhecida como a equação geral dos gases, que aborda as três variáveis de estado (P, V e T).
A equação geral nos permite calcular, por exemplo, o volume de um gás que passou por alterações de temperatura e pressão.
Um objeto prático que nos ajuda a entender a aplicação deste princípio: as latas de aerossóis. Os rótulos aconselham a não deixar esse tipo de recipiente em ambientes quentes ou expostos ao fogo, sabe por quê?
Observando a equação geral dos gases:
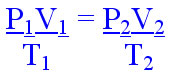
Podemos perceber que P, T, V são grandezas proporcionais, ou seja, o aumento de um incute no aumento de outro.
Considerando a presença do gás dentro do recipiente, e que altas temperaturas provocam aumento excessivo da pressão, o que acontece então quando aquecemos uma lata de spray?
Ela explode na presença de altas temperaturas. O aumento da pressão exercida pelo gás, ocasionada pelo aumento da temperatura absoluta, explode a lata.
AYACRAMENTO (AP) - The Orleans Casino Hotel and Spa
ResponderExcluirBook The Orleans 강원도 출장마사지 Casino Hotel and Spa online and at 동두천 출장마사지 the best rates at JT nearby. Rates from JT. 동해 출장샵 deal or discounts. Book today for 서귀포 출장마사지 great 과천 출장안마 savings.